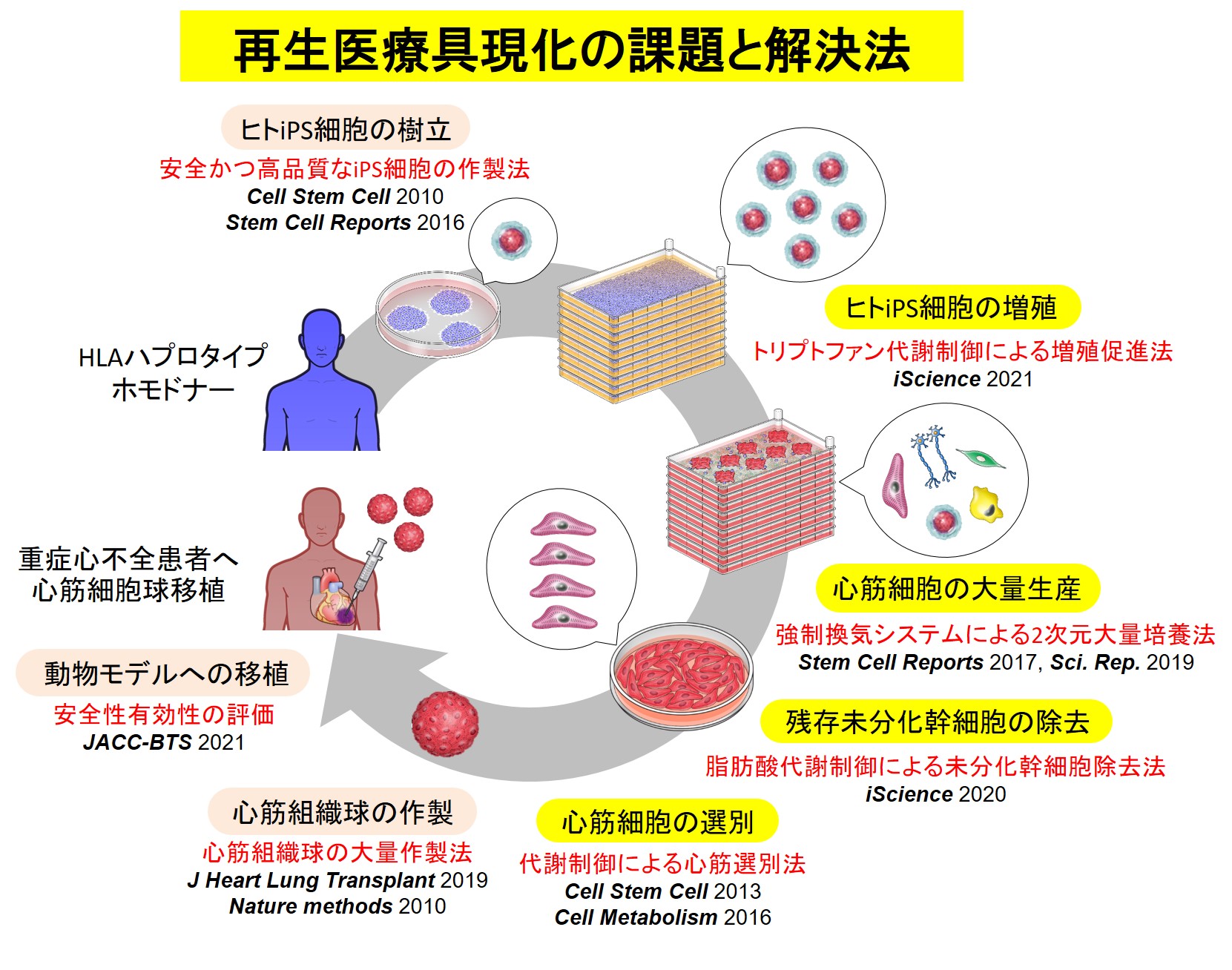
iPS 細胞由来の心筋球による心臓移植に代わる難治性重症心不全治療法を目指して
遠山周吾先生
慶應義塾大学 医学部 循環器内科
Heartseed株式会社 研究開発顧問

遠山 周吾 先生